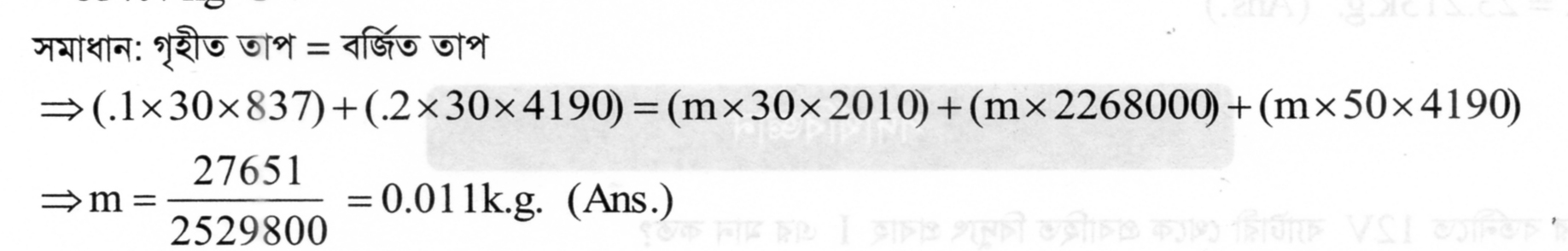100 gm কাঁচের পাত্রে 200 gm পরিমান পানির তাপমাত্র থেকে এ বৃদ্ধি করতে এর তাপমাত্রার কতটুকু ভরের জলীয় বাষ্প প্রয়োজন হবে ? দেওয়া আছে, বাষ্পের আপেক্ষিক তাপ , বাষ্প থেকে পানিতে রূপান্তরের সুপ্ত তাপ পানির আপেক্ষিক তাপ কাঁচের আপেক্ষিক তাপ
ধরা যাক, m ভরের কোনো গ্যাসের আয়তন, চাপ ও পরম তাপমাত্রা যথাক্রমে V, p এবং T।
বয়েলের সূত্র থেকে আমরা পাই, V যখন m এবং T ধ্রুব এবং চার্লসের সূত্র থেকে আমরা পাই, VT, যখন m এবং p ধ্রুব।
অনুপাতের সূত্রানুসারে, যখন m ধ্রুব
pV = KT ….. (10.5)
এখানে K একটি ধ্রুব সংখ্যা, এর মান গ্যাসের ভর, m উপর নির্ভর করে।
যদি T1, T2,…… Tn কেলভিন তাপমাত্রায় এবং P1, P2…. .. Pn চাপে কোনো নির্দিষ্ট ভরের গ্যাসের আয়তন যথাক্রমে V1, V2 .... Vn, হয়, তাহলে উপরিউক্ত সমীকরণ অনুসারে,
ধ্রুবক (10.7)
যদি এক মোল (mole) বা এক গ্রাম অণু গ্যাস বিবেচনা করা হয় তাহলে সকল গ্যাসের জন্য এই ধ্রুব সংখ্যার মান একই হয়। তখন এই ধ্রুবককে R দিয়ে নির্দেশ করা হয়, অন্যক্ষেত্রে একে K দিয়ে প্রকাশ করা হয়।
সুতরাং এক মোল গ্যাসের জন্য
বা, pV = RT
এখানে R হচ্ছে মোলার গ্যাস ধ্রুবক এবং V হচ্ছে এক মোল গ্যাসের আয়তন। অ্যাভোগাড্রোর অনুকম্প অনুসারে অভিন্ন চাপ ও তাপমাত্রায় যেকোনো গ্যাসের এক মোল একই আয়তন দখল করে এবং প্রমাণ তাপমাত্রা ও চাপে এই আয়তন হচ্ছে 22.4 litre বা, 22.4 x 10-3m3। সুতরাং R-এর মান সকল গ্যাসের জন্য একই। এজন্য R-কে সর্বজনীন বা বিশ্বজনীন গ্যাস ধ্রুবক বলে। R-এর মান এস আই বা আন্তর্জাতিক পদ্ধতিতে 8.31 J K-1 mol-1
যদি এক মোল বা এক গ্রাম অণু গ্যাস না নিয়ে m পরিমাণ গ্যাস নেওয়া হয় যার আয়তন V এবং ঐ গ্যাসের আণবিক ভর যদি M হয়, তবে এক মোল বা এক গ্রাম অণু গ্যাসের আয়তন হবে V। সুতরাং ( 10.7) সমীকরণে V এর পরিবর্তে V বসিয়ে আমরা পাই,
বা, pV = RT
কিন্তু হচ্ছে গ্যাসের মোলের সংখ্যা যা পূর্ণ সংখ্যা বা ভগ্নাংশ হতে পারে। একে n দিয়ে প্রকাশ করা হলে উপরিউক্ত
সমীকরণ দাঁড়ায়,
pV =nRT
এ সমীকরণ হচ্ছে বয়েল ও চার্লসের সূত্রের সংযুক্ত রূপ। এ সমীকরণকে সাধারণত গ্যাস সমীকরণ বা আদর্শ গ্যাসের অবস্থার সমীকরণ বলা হয়। কেননা, যেকোনো ভরের গ্যাসের চাপ, আয়তন এবং তাপমাত্রা জেনে এর ভৌত অবস্থা পরিপূর্ণভাবে জানা যায় ।
যে সকল গ্যাস বয়েল ও চার্লসের সূত্র যুগ্মভাবে (অর্থাৎ 10.9 সমীকরণ) মেনে চলে তাদেরকে আদর্শ গ্যাস বলে।
এজন্য (10.9) সমীকরণকে আদর্শ গ্যাস সমীকরণও বলে। বাস্তবে কোনো গ্যাসই আদর্শ গ্যাসের ন্যায় আচরণ করে না। কেবলমাত্র নিম্নচাপ ও উচ্চ তাপমাত্রায় গ্যাস এ সমীকরণ মেনে চলে।